CẬP NHẬT SỰ THAY ĐỔI TRONG LỰA CHỌN PHƯƠNG PHÁP PHẪU THUẬT UNG THƯ TUYẾN GIÁP THỂ BIỆT HOÁ CỦA HIỆP HỘI UNG THƯ TUYẾN GIÁP HOA KỲ NĂM 2025
GS. TS. Mai Trọng Khoa, PGS. TS. Phạm Cẩm Phương, PGS. TS. Phạm Văn Thái, ThS. BSNT. Cao Văn Trung, BSNT. Nguyễn Xuân An
(Tổng hợp)
Ung thư tuyến giáp hiện đang là một vấn đề sức khỏe toàn cầu đáng quan tâm do tỷ lệ mắc gia tăng nhanh chóng. Theo báo cáo mới nhất từ GLOBOCAN 2022, ung thư tuyến giáp đứng thứ 9 về tỷ lệ mắc trong các loại ung thư nói chung, với khoảng 820.000 ca mắc mới được ghi nhận trên toàn thế giới mỗi năm và đứng hàng thứ 21 trong các số các ung thư ở Việt Nam.
Ung thư tế bào biểu mô tuyến giáp bao gồm các thể mô bệnh học chính là ung thư biểu mô tuyến giáp thể nhú (chiếm tỷ lệ khoảng 85%), ung thư biểu mô tuyến giáp thể nang (chiếm 12%) và một số thể hiếm gặp khác. Ung thư tuyến giáp thể biệt hóa (DTC) là loại ung thư tuyến giáp có tiên lượng tốt nhất, bao gồm: ung thư thể nhú (PTC) và thể nang, tế bào Hurthle.
Điều trị ung thư tuyến giáp thể biệt hóa thường cần phối hợp nhiều phương pháp với nhau như phẫu thuật, điều trị bằng Iod phóng xạ (I - 131), liệu pháp hormone, điều trị đích và theo dõi định kỳ. Trong thời gian dài, phẫu thuật cắt toàn bộ tuyến giáp được xem là phương pháp điều trị chính cho hầu hết các khối u có kích thước > 1cm nhằm tối ưu hóa việc điều trị I - 131 và theo dõi bằng Thyroglobulin (Tg). Tuy nhiên, phương pháp này đi kèm với gánh nặng bệnh tật đáng kể như: suy giáp vĩnh viễn, có nguy cơ hạ Canxi máu và liệt dây thanh quản cao hơn so với phẫu thuật bảo tồn.
Trước bối cảnh đó,Hiệp hội Tuyến giáp Hoa Kỳ (ATA) – một trong những hiệp hội uy tín hàng đầu trong chẩn đoán và điều trị bệnh lý tuyến giáp đã có các khuyến cáo mới nhất về điều trị ung thư tuyến giáp vào cuối năm 2025. Khuyến cáo lần này đã có sự chuyển dịch mô hình điều trị sang cá thể hóa và tối ưu hóa can thiệp, đặc biệt là việc mở rộng chỉ định cắt thùy cho nhóm nguy cơ tái phát thấp (ung thư tuyến giáp thể biệt hóa nguy cơ thấp là các khối u có kích thước nhỏ hơn 4 cm và hoàn toàn khu trú trong tuyến giáp). Bài viết này tập trung phân tích cơ sở khoa học, các tiêu chuẩn chỉ định mới trong khuyến cáo về phẫu thuật ung thư tuyến giáp thể biệt hóa của ATA 2025.
1. Tổng quan giải phẫu và các phương pháp phẫu thuật tuyến giáp
1.1. Đặc điểm giải phẫu tuyến giáp
Tuyến giáp nằm phía trong cổ, phía trước khí quản, nằm giữa sụn thanh quản và phần trên tuyến ức,ngang với các đốt sống C5 - T1.
Tuyến giáp có 2 thùy chính là thùy trái và thùy phải nối nhau tại eo tuyến giáp. Mặt sau của cá thùy bên có 4 tuyến cận giáp nằm phía sau. Mạch máu nuôi tuyến giáp gồm hai động mạch giáp trên và hai động mạch giáp dưới.
Dây thần kinh quặt ngược liên quan chặt chẽ với mặt sau tuyến giáp, bắt chéo động mạch giáp dưới.Ở cực trên, dây thần kinh thanh quản trên nằm gần bó mạch giáp trên. Trong phẫu thuật cắt tuyến giáp cần thiết thắt các động mạch và khi thắt cần đặc biệt chú ý để không thắt nhầm các thần kinh này.
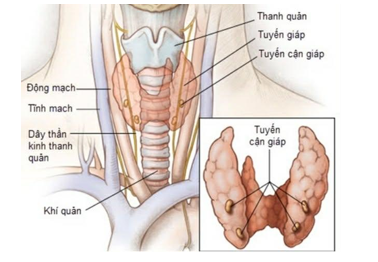
Hình 1: Giải phẫu tuyến giáp
1.2. Các phương pháp phẫu thuật ung thư tuyến giáp
Lựa chọn phương pháp phẫu thuật phụ thuộc vào mức độ của bệnh như kích thước khối u nguyên phát, mức độ xâm lấn ngoài tuyến giáp hoặc di căn hạch, tuổi và các bệnh kết hợp...
Hai phương pháp phẫu thuật thường được sử dụng trong ung thư tuyến giáp biệt hóa gồm:
- Cắt toàn bộ tuyến giáp: loại bỏ hoàn toàn mô giáp, cùng với việc xác định và bảo tồn dây thần kinh quặt ngược, dây thần kinh thanh quản trên và nguồn cấp máu cho các tuyến cận giáp.
- Phẫu thuật cắt thùy và eo: cắt bỏ toàn bộ thùy có u và eo tuyến giáp, không can thiệp vào vùng cổ bên còn lại. Suy cận giáp hiếm khi xảy ra sau phẫu thuật cắt thùy và eo vì không ảnh hưởng đến các tuyến cận giáp bên còn lại. Tương tự, khàn giọng có thể xảy ra do tổn thương thần kinh quặt ngược 1 bên, nhưng phẫu thuật cắt thùy không gây các biến chứng nghiêm trọng do liệt dây thanh 2 bên.

Hình 2: Phương pháp phẫu thuật tuyến giáp
2. Khuyến cáo lựa chọn phương pháp phẫu thuật theo hướng dẫn của ATA 2025
Theo hướng dẫn của Hiệp hội Tuyến giáp Hoa Kỳ năm 2025, phạm vi phẫu thuật ban đầu trong ung thư tuyến giáp biệt hóa (DTC) được xác định dựa trên kích thước u, mức độ xâm lấn tại chỗ, tình trạng di căn hạch và di căn xa, cũng như phân tầng nguy cơ tái phát.
- Bệnh nhân ung thư tuyến giáp có kích thước≤ 2cm, không có xâm lấn đại thể ra ngoài tuyến giáp (cT1) và không có di căn (cN0M0): phẫu thuật ban đầu nên là cắt thùy tuyến giáp nếu không cólý do gì phải phẫu thuật ở thùy còn lại (ví dụ nghi ngờ ung thư tuyến giáp ở thùy còn lại, tiền sử xạ trị vùng đầu - cổ, tiền sử gia đình có nhiều người mắc ung thư tuyến giáp hoặc bệnh nhân không đủ điều kiện theo dõi thích hợp). (Khuyến cáo mạnh, mức độ bằng chứng trung bình).
- Bệnh nhân nguy cơ thấp, ung thư tuyến giáp một bên, kích thước > 2cm và ≤ 4cm (cT2N0M0: cắt thùy tuyến giáp có thể là lựa chọn phẫu thuật ban đầu được ưu tiên, do nguy cơ biến chứng và tác dụng phụ thấp hơn rõ rệt. Tuy nhiên, bệnh nhân và nhóm điều trị có thể lựa chọn cắt toàn bộ tuyến giáp nhằm cho phép điều trị I - 131 và/hoặc cải thiện theo dõi sau điều trị, dựa trên đặc điểm bệnh, sự hiện diện của nhân nghi ngờ ở thùy đối bên và/hoặc nguyện vọng của bệnh nhân. Khi đề xuất cắt thùy tuyến giáp là điều trị ban đầu, cần tư vấn cho bệnh nhân về khả năng phải chuyển sang cắt toàn bộ tuyến giáp trong mổ hoặc phẫu thuật cắt hoàn tất sau mổ nếu xuất hiện các yếu tố nguy cơ cao hơn trong hoặc sau phẫu thuật. (Khuyến cáo có điều kiện, mức độ bằng chứng thấp - trung bình).
- Đối với bệnh nhân ung thư tuyến giáp có kích thước > 4cm, xâm lấn ra ngoài tuyến giáp hoặc di căn: phẫu thuật ban đầu nên là cắt toàn bộ tuyến giáp, trừ khi có chống chỉ định với thủ thuật này. (Khuyến cáo mạnh, mức độ bằng chứng trung bình).
Bảng 1. So sánh khuyến cáo phẫu thuật của ATA 2015 và ATA 2025 đối với ung thư tuyến giáp thể biệt hóa
Theo khuyến cáo của ATA 2025, mức độ cắt bỏ phẫu thuật đối với các khối u nguy cơ thấp đã có sự chuyển đổi sang ưu tiên bảo tồn và cá thể hoá người bệnh. Trong khi đó hướng dẫn ATA 2015 chỉ xem xét phẫu thuật cắt thùy như một lựa chọn thay thế cho các khối u kích thước 1 - 4cm, ATA 2025 đã tái định vị phương pháp này trở thành chỉ định ưu tiên cho nhóm nguy cơ thấp. Sự thay đổi này được củng cố bởi các dữ liệu y học chứng cứ khẳng định tính tương đương về tỷ lệ sống còn toàn bộ giữa cắt thùy và cắt toàn bộ tuyến giáp, đồng thời nhấn mạnh lợi ích vượt trội của bảo tồn trong việc giảm thiểu biến chứng và tối ưu hóa chất lượng cuộc sống.
Những hiểu biết sâu hơn về cơ chế phân tử thúc đẩy khả năng xâm lấn của khối u cho phép cá thể hóa hơn nữa trong tương lai vẫn đang được nghiên cứu, đặc biệt liên quan đến các bệnh nhân mắc DTC mà mức độ phẫu thuật vẫn chưa rõ ràng. Theo hướng dẫn số 10 của ATA 2025: xét nghiệm phân tử tiền phẫu chưa được khuyến cáo thường quy, tuy nhiên trong trường hợp đã có kết quả, sự hiện diện hoặc vắng mặt của một số tổ hợp gen có thể xem xét như yếu tố hỗ trợ, kết hợp với lâm sàng và nguyện vọng bệnh nhân nhằm quyết định mức độ phẫu thuật ban đầu (Khuyến cáo có điều kiện, mức độ bằng chứng thấp).
Dựa trên các dữ liệu hồi cứu và phân tích quan sát hiện có, một số đặc điểm phân tử đã được ghi nhận có liên quan đến khả năng xâm lấn và tái phát của khối u. Các đột biến phân tử nguy cơ thấp như RAS và giống RAS thường liên quan đến các khối u ít xâm lấn và có thể phù hợp với chiến lược phẫu thuật bảo tồn. Ngược lại, một số tổ hợp đột biến nguy cơ cao như TERT, TP53, AKT1, PIK3CA gợi ý hành vi xâm lấn mạnh của khối u từ đó cân nhắc phẫu thuật triệt căn. Tuy nhiên, vai trò các yếu tố phân tử hiện nay chủ yếu mang tính hỗ trợ và chưa đủ bằng chứng để sử dụng một cách độc lập.
3. Cơ sở bằng chứng của ATA 2025
3.1. Tỷ lệ sống thêm và tái phát
ATA 2015 đã khuyến cáo rằng phẫu thuật cắt toàn bộ tuyến giáp hoặc cắt thùy đều chấp nhận được đối với DTC nguy cơ thấp dựa trên nghiên cứu của Adam và cộng sự được công bố vào năm 2014, các tác giả khẳng định không có sự khác biệt có ý nghĩa thống kê về tỷ lệ sống thêm toàn bộ giữa cắt thùy và cắt toàn bộ tuyến giáp đối với các khối u có kích thước từ 1 đến 4 cm.
Kể từ khi xuất bản hướng dẫn năm 2015,nhiều nghiên cứu đã được công bố để đánh giá khuyến nghị này. Zhang và cộng sự (2020) đã tổng hợp dữ liệu được phân tích gộp của 13 nghiên cứu so sánh trực tiếp hiệu quả giữa phẫu thuật cắt toàn bộ tuyến giáp và phẫu thuật bảo tồn (cắt thùy) trên bệnh nhân ung thư tuyến giáp thể nhú (PTC), kết quả chỉ ra rằng không có sự khác biệt có ý nghĩa thống kê về tỷ lệ sống còn toàn bộ (Overall Survival) giữa hai phương pháp phẫu thuật, đặc biệt ở nhóm bệnh nhân có kích thước khối u dưới 2 cm.
3.2. Đánh giá về độ an toàn, biến chứng và chất lượng cuộc sống sau phẫu thuật
Cở sở lý luận cho việc ưu tiên bảo tồn trong điều trị DTC nguy cơ thấp còn dựa trên rủi ro của cắt toàn bộ tuyến giáp lớn hơn đáng kể so với cắt thùy. Hauch và cộng sự phân tích chéo dữ liệu của 62.722 ca phẫu thuật tuyến giáp từ cơ sở dữ liệu Nationwide Inpatient Sample(2003–2009), so sánh biến chứng sau cắt toàn bộ tuyến giáp và cắt thuỳ, kết quả cho thấy nhóm cắt toàn bộ có nguy cơ xảy ra biến chứng sau mổ cao hơn cắt thuỳ(20,8% so với 10,8%). Rosato và cộng sự tổng hợp báo cáo từ cơ sở dữ liệu quốc gia Ý có kết quả rằng tỷ lệ suy cận giáp vĩnh viễn sau cắt toàn bộ là 2,8%,trong khi ở cắt thùy là 0%.
Năm 2022, Chen và cộng sự đã công bố một nghiên cứu ghi nhận rằng bệnh nhân cắt toàn bộ tuyến giáp chịu gánh nặng tâm lý và thể chất (lo âu, trầm cảm, mệt mỏi, thay đổi giọng nói) cao hơn đáng kể trong giai đoạn hậu phẫu sớm so với nhóm cắt thùy.Mặc dù sự khác biệt này có thể thu hẹp sau 6 - 12 tháng, nhưng lợi ích ngắn hạn và việc tránh phụ thuộc hormon thay thế trọn đời là ưu điểm rõ rệt của phẫu thuật bảo tồn.
Như vậy, qua những nghiên cứu chứng minh tỷ lệ sống thêm tương đương giữa bệnh nhân DTC nguy cơ thấp được điều trị bằng cắt thùy so với cắt toàn bộ, việc mở rộng chỉ định ưu tiên bảo tồn để nâng cao chất lượng của sống của bệnh nhân theo ATA 2025 là đặc biệt quan trọng.
3.3. Ứng dụng các yếu tố tiên lượng phân tử và nguyện vọng của bệnh nhân trong thiết lậpkế hoạch phẫu thuật ban đầu
Song song với các yếu tố lâm sàng, nhiều nghiên cứu gần đây đã làm rõ vai trò của sinh học phân tử trong việc dự đoán mức độ xâm lấn và nguy cơ tái phát của ung thư tuyến giáp và do đó hướng phẫu thuật viên đến cắt bỏ toàn bộ tuyến giáp. Kurtom và cộng sự (2025) nghiên cứu trên các bệnh nhân được chẩn đoán DTC nguy cơ thấp và đã trải qua phẫu thuật ban đầu cho thấy các khối u mang đột biến nguy cơ trung gian và cao (BRAF V600E đơn thuần, TERT, TP53, AKT1, PIK3CA) có tỷ lệ tái phát cao rõ rệt (7,2%), đặc biệt khi kích thước khối u > 2cm. Ngược lại, các khối u có gen RAS và giống RAS có tỷ lệ tái phát rất thấp (0,7%).
Tuy nhiên, Schumm và cộng sự đã nghiên cứu 105 bệnh nhân PTC có kết quả tế bào học Bethesda V - VI, được thực hiện xét nghiệm phân tử trước phẫu thuật. Kết quả cho thấy nhóm đột biến nguy cơ cao TERT chỉ chiếm 6%, và đa phần ở nhóm bệnh đã tiến triển tại chỗ hoặc di căn.Điều này cho thấy các đột biến phân tử nguy cơ cao hiếm gặp ở DTC giai đoạn sớm, và giá trị của xét nghiệm phân tử thường quy trong nhóm này còn hạn chế.
Trong tương lai, khi các nghiên cứu về chi phí - hiệu quả về xét nghiệm phân tử đầy đủ, kiểu gen khối u có thể đóng vai trò ngày càng quan trọng trong việc xác định mức độ phẫu thuật tối ưu cho bệnh nhân DTC nguy cơ thấp.
ATA 2025 còn hướng tới cá thể hóa điều trị thông qua nguyện vọng của bệnh nhân trong lựa chọn phương pháp phẫu thuật ban đầu. Ở góc độ người bệnh, nghiên cứu của Lubitz CC và cộng sự trên 1546 bệnh nhân DTC nguy cơ thấp cung cấp bằng chứng rằng bệnh nhân mong muốn được tham gia vào quyết định điều trị, trong đó 1 tỷ lệ đáng kể sẵn sàng lựa chọn cắt thùy (39%) hoặc thậm chí theo dõi chủ động (35%) nếu kết cục ung thư không thay đổi.
4. Kết luận
Sự chuyển dịch từ hướng dẫn ATA 2015 sang bản cập nhật hướng tới 2025 đánh dấu một bước tiến quan trọng trong tư duy điều trị ung thư tuyến giáp biệt hóa: sự chuyển dịch mô hình mạnh mẽ sang cá thể hóa và tối ưu hóa can thiệp.
Việc mở rộng chỉ định cắt thùy cho các khối u ở nhóm nguy cơ thấp được củng cố bởi các bằng chứng y học mức độ cao, khẳng định sự an toàn về mặt ung bướu học với tỷ lệ sống thêm và kiểm soát bệnh tương đương phẫu thuật cắt toàn bộ. Chiến lược này mang lại lợi ích kép: vừa giải phóng bệnh nhân khỏi gánh nặng của các biến chứng (suy cận giáp, liệt dây thanh), vừa bảo tồn chức năng nội tiết tự nhiên, từ đó cải thiện đáng kể chất lượng cuộc sống.
Tuy nhiên, để áp dụng thành công hướng dẫn mới, thực hành lâm sàng tại Việt Nam cần vượt qua những thách thức về chẩn đoán giai đoạn chính xác và tư vấn người bệnh. Phẫu thuật cắt thùy không phải là sự thỏa hiệp về kết quả điều trị, mà là sự lựa chọn tinh tế đòi hỏi sự phối hợp chặt chẽ giữa chẩn đoán hình ảnh, giải phẫu bệnh và phẫu thuật viên, cùng sự tuân thủ theo dõi nghiêm ngặt của người bệnh. Đây chính là nền tảng cho một kỷ nguyên điều trị ung thư tuyến giáp an toàn, hiệu quả và nhân văn hơn.
Tài liệu tham khảo:
1. Lê Ngọc Hà. Điều trị và quản lý ung thư tuyến giáp thể biệt hoá sau phẫu thuật (Sách chuyên khảo). Nhà xuất bản Y học.
2. Haugen BR,Alexander EK, Bible KC, et al. 2015 American Thyroid Association managementguidelines for adult patients with thyroid nodules and differentiated thyroidcancer. Thyroid. 2016;26(1):1–133.
3. American Thyroid Association. ATA clinical practice guidelines for the management ofdifferentiated thyroid cancer: 2025 update. Thyroid. 2025.
4. Adam MA, PuraJ, Gu L, et al. Extent of surgery for papillary thyroid cancer is notassociated with survival. Ann Surg. 2014;260(4):601–607.
5. Zhang L, WeiWJ, Ji QH, et al. Comparison of total thyroidectomy and lobectomy for papillarythyroid cancer: a meta-analysis. Oncotarget. 2020.
6. Hauch A,Al-Qurayshi Z, Randolph G, Kandil E. Total thyroidectomy is associated withincreased risk of complications compared with lobectomy. Ann Surg Oncol.2014.
7. Rosato L,Avenia N, Bernante P, et al. Complications of thyroid surgery: analysis of amulticentric study on 14,934 patients operated on in Italy. Ann Surg.2004.
8. Chen Y, Li X,Wu Y, et al. Quality of life after total thyroidectomy versus lobectomy inpatients with differentiated thyroid cancer. J Surg Oncol. 2022.
9. Kurtom S, Liu JB, Doerfler WR, Calcaterra M, McCoy KL,Sada A, et al. Tumor size and molecular risk group are associated withdifferentiated thyroid cancer recurrence. Surgery. 2025.
10. Schumm MA, Phillips JM, Haidar YM, et al. Moleculartesting in Bethesda V–VI papillary thyroid carcinoma and implications forsurgical management. Thyroid. 2020.
11. Lubitz CC, Roman SA, Alexander EK, et al. Patientpreferences for extent of surgery in low-risk thyroid cancer. Thyroid.2014.